| Сульфат лития | |
|---|---|
 |
|
| Сульфат лития | |
| Традиционные названия | Сернокислый литий |
| Хим. формула | Li2SO4 |
| Молярная масса | 109,94 г/моль |
| Плотность | 2,221 г/см³ |
| Температура | |
| • плавления | 859 °C |
| Мол. теплоёмк. | 117,57 Дж/(моль·К) |
| Энтальпия | |
| • образования | -1436,0 кДж/моль |
| Удельная теплота плавления | 9,3 кДж/моль |
| Растворимость | |
| • в воде | 34,320; 29,2100 г/100 мл |
| Рег. номер CAS | 10377-48-7 |
| PubChem | 66320 |
| Рег. номер EINECS | 233-820-4 |
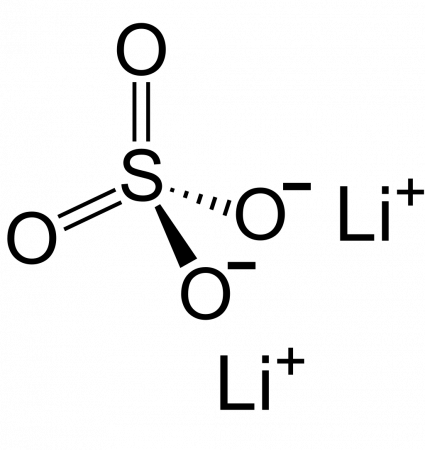
| SMILES | [Li+].[Li+].[O-]S(=O)(=O)[O-] |
| InChI | 1S/2Li.H2O4S/c;;1-5(2,3)4/h;;(H2,1,2,3,4)/q2*+1;/p-2INHCSSUBVCNVSK-UHFFFAOYSA-L |
| RTECS | OJ6419000 |
| ChEBI | 53474 |
| ChemSpider | 59698 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. |
Сульфат лития — соль щелочного металла лития и серной кислоты. Химическая формула Li2SO4. Образует кристаллогидрат Li2SO4•H2O.
Получение
- Кристаллогидрат сульфата лития получают взаимодействием гидроксида или карбоната лития с серной кислотой с последующим упариванием:
- 2 LiOH + H2SO4 → Li2SO4 + 2 H2O
- Безводную соль получают нагреванием моногидрата выше 500°С.
Физические свойства
Безводный сульфат лития образует три кристаллические модификации:
- α-форма — устойчивая при обычных условиях модификация с моноклинной решёткой, пространственная группа P 21/c, параметры a = 0,844 нм, b = 0,495 нм, c = 0,824 нм, β = 107,9°, Z = 4.
- β-форма — гексагональная решётка
- γ-форма — при температуре выше 575°С образует кубическую решётку, пространственная группа I43m, a = 0,707 нм, Z = 4.
Кристаллогидрат образует кристаллы моноклинной сингонии, пространственная группа P 21, параметры a = 0,814 нм, b = 0,483 нм, c = 0,543 нм, β = 107,58°, Z = 4.
Химические свойства
- Взаимодействует с серной кислотой с образованием гидросульфата лития:
- Li2SO4 + H2SO4 → 2 LiHSO4
- Взаимодействием с соединениями бария удобно получать различные соединения лития:
- Li2SO4 + Ba(OH)2 → 2 LiOH + BaSO4↓
- Li2SO4 + Ba(N3)2 → 2 LiN3 + BaSO4↓
- При нагревании с водородом, аммиаком или углеродом (кокс) восстанавливается до сульфида лития:
- Li2SO4 + 4 C →800oC Li2S + 4 CO
Применение
Сульфат лития используется для изготовления головок детекторов в ультразвуковой дефектоскопии и как компонент люминофоров. Также он используется как средство для лечения маниакально-депрессивного психоза. Это вещество — пьезоэлектрик.
Физиологическое действие
Сульфат лития обладает средней токсичностью. Как и все соединения лития, влияет на ЦНС.
| Соединения лития |
|---|
| __ Li + __ S 6+ __ O 2- | |
| имена | |
|---|---|
| название IUPACлитий сульфат | |
| Другие имена сульфат Lithium | |
| Идентификаторы | |
| Количество CAS | |
| номер RTECS | OJ6419000 |
| UNII |
|
InChI
|
|
УСМЕДЕТСЯ
|
|
| свойства | |
| Химическая формула | Li 2 SO 4 |
| Молярная масса | 109,94 г / моль |
| Внешность | Белый кристаллический твердый, гигроскопичен |
| плотность | 2,221 г / см 3 (безводный) 2,06 г / см 3 (моногидрат) |
| Температура плавления | 859 ° С (1578 ° F, 1 132 К) |
| Точка кипения | +1377 ° С (2511 ° F; 1 650 К) |
| Растворимость в воде | моногидрат: 34,9 г / 100 мл (25 ° С) 29,2 г / 100 мл (100 ° С) |
| Растворимость | нерастворим в абсолютном этаноле , ацетоне и пиридине |
| Магнитная восприимчивость (χ) | —40.0 · 10 -6 см 3 / моль |
| Показатель преломления ( п D ) | 1,465 (β-форма) |
| Состав | |
| Кристальная структура | Примитивный моноклинная |
| Пространственная группа | Р 2 1 / а, № 14 |
| постоянная решетки | = 8,239 Å, б = 4,954 Å, с = 8,474 Å ,а = 90 °, В = 107.98 °, у = 90 ° |
| Решетка объем ( V ) | 328,9 Å 3 |
| Формула единиц ( Z ) | 4 |
| геометрии координации | Тетраэдрическая у серы |
| термохимия | |
| Теплоемкость ( С ) | 1,07 Дж / г К |
| ( S |
113 Дж / моль К |
| (Δ F H |
-1436,37 кДж / моль |
| Свободная энергия Гиббса (Δ F G ˚) | -1324.7 кДж / моль |
| опасности | |
| NFPA 704 | <map>2 |
| Смертельная доза или концентрация ( LD , LC ): | |
| LD 50 ( средняя доза ) | 613 мг / кг (крыса, перорально) |
| Родственные соединения | |
| Другие катионы | Сульфат натрия сульфат калия |
| За исключением случаев, когда указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| N проверить ( что ?) YN | |
| ссылки Infobox |
Сульфат Лития представляет собой белую неорганическую соль с формулой Li 2 S O 4 . Это лития соль из серной кислоты .
свойства
Физические свойства
Сульфат Литий является растворимым в воде, но из этого не следует обычной тенденции растворимости в зависимости от температуры — его растворимость в воде уменьшается с ростом температуры, так как его растворение является эндотермическим процессом. Это свойство является общим с несколькими неорганическими соединениями , такими как лантаноидов сульфатами .
Кристаллы сульфата Лития, будучи пьезоэлектрическим , также используется в ультразвуковом типе неразрушающего контроля , потому что они являются очень эффективными звуковыми приемниками. Тем не менее, они страдают в этом применении из — за их растворимости в воде.
Поскольку она имеет гигроскопические свойства , наиболее распространенной формой сульфата лития моногидрата сульфата лития. Безводный сульфат лития имеет плотность 2,22 г / см 3 , но, взвешивая лития сульфат безводный может стать громоздким , как это должно быть сделано в воде не хватает атмосферы.
Сульфат Литий имеет пироэлектрические свойства . Когда водный раствор лития сульфатированная нагреваются, электропроводность также увеличивается. Молярность сульфата лития также играет определенную роль в электрической проводимости; оптимальная проводимость достигается при 2М , а затем уменьшается.
Когда твердое сульфат лития растворяют в воде она имеет эндотермическую диссоциацию . Это отличается от сульфата натрия , который имеет экзотермическую диссоциацию. Точная энергия диссоциации трудно количественно оценить , как это кажется относительно молей добавленной соли. Небольшие количества растворенного сульфата лития имеет значительно большее изменение температуры , чем большие количества.
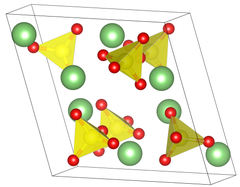
кристаллические свойства
Сульфат литий имеет два различных кристаллических фаз . В общей форме фазы II, сульфат литий имеет клиновидную моноклинную кристаллическую систему , которая имеет длины ребер а = 8.23Å б = 4.95Å с = 8.47Å β = 107.98 °. Когда сульфат лития с подогревом прошло 130 ℃ он переходит в свободное состояние воды , но сохраняет свою кристаллическую структуру. Это не до 575 ℃ , когда происходит преобразование из фазы II в фазу I. Изменения кристаллической структуры к гранецентрированной кубической сингонии , с длиной ребра 7.07Å. Во время этого изменения фазы, плотность изменений сульфата лития от 2,22 до 2,07 г / см 3 .
Пользы
Сульфат лития используется для лечения биполярного расстройства (см фармакологию лития ).
Сульфат литии исследован в качестве потенциального компонента ионной проводимости стекол. Прозрачная проводящая пленка является весьма исследовалась тема , поскольку они используются в таких приложениях, как солнечные батареи и потенциал для нового класса батареи. В этих случаях, важно иметь высокое содержание лития; более широко известный двоичный борат лития (Li₂O · B₂O₃) трудно получить с высокой концентрацией литии и трудно сохранить , поскольку это является гигроскопичным. С добавлением сульфата лития в систему, легко получить, стабильная, высокая концентрация лития стекла может быть сформирован. Большинство современных прозрачных ионных проводящих пленок из органических полимерных материалов , и было бы идеально , если бы недорогое стабильное неорганическое стекло может быть разработано.
Сульфат лития был испытан в качестве добавки для портландцемента для ускорения отверждения с положительными результатами. Сульфат Лития служит для ускорения реакции гидратации (см цемента ) , который уменьшает время отверждения. Беспокойство с уменьшением времени отверждения является прочность конечного продукта, но при испытании, сульфат лития , легированного Портландцемент не имели заметного снижения прочности.
медикаментозное лечение
Литий (Li) используется в психиатрии для лечения мании , эндогенной депрессии, психоза и; а также для лечения шизофрении. Как правило , карбонат лития (Li₂CO₃) применяется, но иногда лития цитрат (Li₃C 6 Н 5 О 7 ), сульфат лития или оксибутират лития используются в качестве альтернативы. Ли не метаболизируется. Из — за Ли химическое сходство с натрий (Na +) и калий (K +), он может взаимодействовать или мешать биохимическими путями для этих веществ и смещает эти катионы из внутри- или внеклеточных отсеков тела. Ли , кажется, транспортируют из нервных и мышечных клеток с помощью активного насоса натрия, хотя нерационально.
Литий сульфат имеет быстрое желудочно — кишечного тракта скорость абсорбции ( в течение нескольких минут) и полное после перорального введения таблетки или жидкой форме. Он быстро проникает в печень и почки , но требует 8-10 дней , чтобы достичь телесного равновесия. Li производит много метаболических изменений и нейроэндокринные, но никаких убедительных доказательств не выступает один конкретный способом действия. Например, литий взаимодействует с нейрогормонами, в частности биогенных аминов , серотонин (5-гидрокси триптамин) и норэпинефриной , который обеспечивает вероятный механизм для полезных эффектов в психиатрических расстройствах, например , маний . В ЦНС , Ли влияет нерва возбуждение, синаптическую передачу и метаболизм нейронов. Li стабилизирует серотонинергической нейротрансмиссии.
Реакции
Литий сульфат был использован в органическом синтезе химии. сульфат лития используется в качестве катализатора для реакции элиминирования в изменяющемся н-бутилбромида к 1-бутена при близкой к 100% урожайности в диапазоне от 320 ℃ до 370 ℃. Выход этой реакции резко изменяется при нагревании за пределами этого диапазона, как более высокие выходы 2-бутено образуются.
Рекомендации
Используемые источники:
- https://chem.ru/sulfat-litija.html
- https://ru.qwe.wiki/wiki/lithium_sulfate

 Литий-титанатные аккумуляторы ( LTO ) и его виды
Литий-титанатные аккумуляторы ( LTO ) и его виды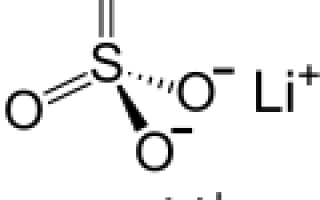

 Литий-ионный аккумулятор 18650: размеры. Аккумулятор 18650: применение
Литий-ионный аккумулятор 18650: размеры. Аккумулятор 18650: применение Lifepo4 аккумуляторы эксплуатация и особенности
Lifepo4 аккумуляторы эксплуатация и особенности Выбор li-ion аккумулятора 18650 для шуруповерта
Выбор li-ion аккумулятора 18650 для шуруповерта История типоразмеров электрических батарей
История типоразмеров электрических батарей