Об элементе
Ли́тий (химический символ — Li; лат. Lithium) — элемент первой группы (по устаревшей классификации — главной подгруппы первой группы), второго периода периодической системы химических элементов с атомным номером 3.
Литий был открыт в 1817 году шведским химиком и минералогом Иоганном Арфведсоном сначала в минерале петалите (Li,Na)[Si4AlO10], а затем в сподумене LiAl[Si2O6] и в лепидолите KLi1.5Al1.5[Si3AlO10](F,OH)2. Металлический литий впервые получил Гемфри Дэви в 1818 году.
Своё название литий получил из-за того, что был обнаружен в «камнях» (греч. λίθος — камень). Первоначально назывался «литион», современное название было предложено Берцелиусом.
Физические свойства
Простое вещество литий — мягкий щелочной металл серебристо-белого цвета, , мягкий и пластичный, твёрже натрия, но мягче свинца. Его можно обрабатывать прессованием и прокаткой.
При комнатной температуре металлический литий имеет кубическую объёмноцентрированную решётку (координационное число 8), пространственная группа I m3m, параметры ячейки a = 0,35021 нм, Z = 2. Ниже 78 К устойчивой кристаллической формой является гексагональная плотноупакованная структура, в которой каждый атом лития имеет 12 ближайших соседей, расположенных в вершинах кубооктаэдра. Кристаллическая решетка относится к пространственной группе P 63/mmc, параметры a = 0,3111 нм, c = 0,5093 нм, Z = 2.
Маленькие размеры атома лития приводят к появлению особых свойств металла. Например, он смешивается с натрием только при температуре ниже 380 °C и не смешивается с расплавленными калием, рубидием и цезием, в то время как другие па́ры щелочных металлов смешиваются друг с другом в любых соотношениях.
Химические свойства
Литий является щелочным металлом, однако относительно устойчив на воздухе. Литий является наименее активным щелочным металлом, с сухим воздухом (и даже с сухим кислородом) при комнатной температуре практически не реагирует. По этой причине литий является единственным щелочным металлом, который не хранят в керосине (к тому же плотность лития столь мала, что он будет в нём плавать); он может непродолжительное время храниться на воздухе.
Во влажном воздухе медленно реагирует с азотом и другими газами, находящимися в воздухе, превращаясь в нитрид Li3N, гидроксид LiOH и карбонат Li2CO3. В кислороде при нагревании горит, превращаясь в оксид Li2O. Интересная особенность лития в том, что в интервале температур от 100 °C до 300 °C он покрывается плотной оксидной плёнкой и в дальнейшем не окисляется. В отличие от остальных щелочных металлов, дающих стабильные надпероксиды и озониды; надпероксид и озонид лития — нестабильные соединения.
В 1818 немецкий химик Леопольд Гмелин установил, что литий и его соли окрашивают пламя в карминово-красный цвет, это является качественным признаком для определения лития. Температура самовоспламенения находится в районе 300 °C. Продукты горения раздражают слизистую оболочку носоглотки.
Спокойно, без взрыва и возгорания, реагирует с водой, образуя LiOH и H2. Реагирует также с этиловым спиртом (с образованием алкоголята), с водородом (при 500—700 °C) с образованием гидрида лития, с аммиаком и с галогенами (с иодом — только при нагревании). При 130 °C реагирует с серой с образованием сульфида. В вакууме при температуре выше 200 °C реагирует с углеродом (образуется ацетиленид). При 600—700 °C литий реагирует с кремнием с образованием силицида. Химически растворим в жидком аммиаке (−40 °C), образуется синий раствор.
В водном растворе литий имеет самый низкий стандартный электродный потенциал (−3,045 В) из-за малого размера и высокой степени гидратации иона лития.
Длительно литий хранят в петролейном эфире, парафине, газолине и/или минеральном масле в герметически закрытых жестяных коробках. Металлический литий вызывает ожоги при попадании на влажную кожу, слизистые оболочки и в глаза.
Применение
Сплав сульфида лития и сульфида меди — эффективный полупроводник для термоэлектропреобразователей (ЭДС около 530 мкВ/К).
Из лития изготовляют аноды химических источников тока (аккумуляторов, например, литий-хлорных аккумуляторов) и гальванических элементов с твёрдым электролитом (например, литий-хромсеребряный, литий-висмутатный, литий-окисномедный, литий-двуокисномарганцевый, литий-иодсвинцовый, литий-иодный, литий-тионилхлоридный, литий-оксидванадиевый, литий-фторомедный, Литий-двуокисносерный элементы), работающих на основе неводных жидких и твёрдых электролитов (тетрагидрофуран, пропиленкарбонат, метилформиат, ацетонитрил).
Кобальтат лития и молибдат лития показали лучшие эксплуатационные свойства и энергоёмкость в качестве положительного электрода литиевых аккумуляторов.
Гидроксид лития используется как один из компонентов для приготовления электролита щелочных аккумуляторов. Добавление гидроксида лития к электролиту тяговых железо-никелевых, никель-кадмиевых, никель-цинковых аккумуляторных батарей повышает их срок службы в 3 раза и ёмкость на 21 % (за счёт образования никелатов лития).
Алюминат лития — наиболее эффективный твёрдый электролит (наряду с цезий-бета-глинозёмом).
Монокристаллы фторида лития используются для изготовления высокоэффективных (КПД 80 %) лазеров на центрах свободной окраски и для изготовления оптики с широкой спектральной полосой пропускания.
Перхлорат лития используют в качестве окислителя.
Сульфат лития используют в дефектоскопии.
Нитрат лития используют в пиротехнике для окрашивания огней в красный цвет.
Сплавы лития с серебром и золотом, а также медью являются очень эффективными припоями. Сплавы лития с магнием, скандием, медью, кадмием и алюминием — новые перспективные материалы в авиации и космонавтике (из-за их лёгкости). На основе алюмината и силиката лития создана керамика, затвердевающая при комнатной температуре и используемая в военной технике, металлургии, и, в перспективе, в термоядерной энергетике. Огромной прочностью обладает стекло на основе литий-алюминий-силиката, упрочняемого волокнами карбида кремния. Литий очень эффективно упрочняет сплавы свинца и придает им пластичность и стойкость против коррозии.
Триборат лития-цезия используется как оптический материал в радиоэлектронике. Кристаллические ниобат лития LiNbO3 и танталат лития LiTaO3 являются нелинейными оптическими материалами и широко применяются в нелинейной оптике, акустооптике и оптоэлектронике.Литий также используется при наполнении осветительных газоразрядных металлогалогеновых ламп.Гидроксид лития добавляют в электролит щелочных аккумуляторов для увеличения срока их службы.
В чёрной и цветной металлургии литий используется для раскисления и повышения пластичности и прочности сплавов. Литий иногда применяется для восстановления методами металлотермии редких металлов.
Изотопы 6Li и 7Li обладают разными ядерными свойствами (сечение поглощения тепловых нейтронов, продукты реакций) и сфера их применения различна. Гафниат лития входит в состав специальной эмали, предназначенной для захоронения высокоактивных ядерных отходов, содержащих плутоний.
Высокогигроскопичные бромид LiBr и хлорид лития LiCl применяются для осушения воздуха и других газов.
Соли лития обладают нормотимическими и другими лечебными свойствами. Поэтому они находят применение в медицине.
Стеарат лития («литиевое мыло») используется в качестве загустителя для получения пастообразных высокотемпературных смазок машин и механизмов.
Гидроксид лития LiOH, пероксид Li2O2 применяются для очистки воздуха от углекислого газа; при этом последнее соединение реагирует с выделением кислорода (например, 2Li2O2 + 2CO2 → 2Li2CO3 + O2), благодаря чему используется в изолирующих противогазах, в патронах для очистки воздуха на подлодках, на пилотируемых космических аппаратах и т. д.
Литий и его соединения широко применяют в силикатной промышленности для изготовления специальных сортов стекла и покрытия фарфоровых изделий.
Соединения лития используются в текстильной промышленности (отбеливание тканей), пищевой (консервирование) и фармацевтической (изготовление косметики).
Lithium. Nirvana
Я так счастлив,Ведь сегодня я нашёл своих друзей…Они в моей голове.Я такой безобразный, но это нормально,Ведь и ты такой…Мы разбили наши зеркала.Утро воскресенья.Для меня каждый день.И я не боюсь, зажги мои свечи…Я в оцепенении, ведь я нашёл бога…
Да…
Я так одинок, но это ничего,Я побрил себе голову… И я не печалюсь,И, может,Я виноват во всём, что слышал…Но я не уверен..Я так взвинчен,Не дождусь встречи с тобой там…Мне всё равно.Я так возбужден,Но это не страшно,У меня добрые намерения.
Да..
Я люблю это — я не схожу с умаЯ скучаю по тебе, я не схожу с ума,Я люблю тебя, я не схожу с ума,Я убью тебя, я не схожу с ума..
Я так счастлив,Ведь сегодня я нашёл своих друзей…Они в моей голове.Я такой безобразный, но это нормально,Ведь и ты такой…Мы разбили наши зеркала.Утро воскресенья.Для меня каждый день.И я не боюсь, зажги мои свечи…Я в оцепенении, ведь я нашёл бога…
Да…
Я люблю это — я не схожу с умаЯ скучаю по тебе, я не схожу с ума,Я люблю тебя, я не схожу с ума,Я убью тебя, я не схожу с ума…
Lithium. Evanescence
Литий, не хочу замыкаться в себеЛитий, не хочу забывать, каково остаться без всегоЛитий, хочу остаться влюбленной в свое гореО, но Боже я хочу расслабиться
Ложись в кровать, не заставляй меня спать однойНе смогла спрятать пустоту, ты открыл еёНикогда не хотела испытать такой холод… Просто ты Недостаточно выпил, чтобы сказать, что любишь меня
Я не могу оставаться собойИнтересно, что не так со мной?
Литий, не хочу замыкаться в себеЛитий, не хочу забывать, каково остаться без всегоЛитий, хочу остаться влюбленной в свое горе
В этот раз я не хочу быть сломленной,Подавляю свое желание вырваться.Здесь, в темноте, я знаю себя: я не смогуОсвободиться, пока не расслаблюсь, расслаблюсь…
Дорогой, все же я тебя прощаюЧто угодно лучше, чем остаться однойИ, кажется, что я должна была упасть, в конце концовЯ всегда нахожу себе место среди пепла…
Я не могу оставаться собойИнтересно, что не так со мной?
Литий, не хочу замыкаться в себеЛитий, не хочу забывать, каково остаться без всегоЛитий, хочу остаться влюбленной м-м-мЯ расслаблюсь…
Описание и свойства лития
Литий – элемент, с отношением к первой группе, во втором периоде таблицы, его атомный номер – 3. Формула лития — Li2O. Элемент открыли в 1817 г., был произведён только 1825 г. Название дословно переводится как В«каменьВ».

Литий – это металл, с щелочными свойствами, серебристого цвета, обладающий выраженными пластичными свойствами. Легко поддаётся обработке. Характерен наиболее большой температурой плавления, это 180,54Вє С, кипения — 1340Вє С и низкой плотностью по сравнению с остальными металлами щелочного ряда. Его плотность ниже плотности воды. Это позволяет ему оставаться на плаву на водной поверхности и даже в керосине.
Атом лития своими небольшими размерами позволяет металлу выказывать определённые свойства. Смешение с натрием происходит только в определённой температуре,а с цезием, рубидием и кадмием, он не смешиваться вовсе. Остальные металлы этого ряда подобными свойствами не обладают.
Не смотря на то, что литий это металл с щелочных свойств, он наименее активный из всех прочих, и с кислородом не взаимодействует, с сухим тоже. Поэтому хранить его в керосине, защищая от взаимодействия с кислородной средой, как это делается с другим щелочным металлам, нет необходимости.
К тому же это бесполезно – на практике он всё равно всплывёт на поверхность. Поэтому его можно спокойно хранить на открытом воздухе длительное время, не опасаясь, что в нём произойдут нежелательные изменения.
При достаточной влажности происходит реакция с азотом и другими газами, растворёнными в воздухе. Превращения зависят от свойств контактирующего агента (газа). Может образоваться гидроксид, карбонат или нитрит лития. В процессе нагревания в кислородной среде образуется оксид лития Li2O.
Определить литий несложно – оказавшись в открытом пламени, он окрашивает его своеобразными красными оттенками. Самовоспламеняется при 300Вє С. Следует быть осторожным при этих процессах, так как продукты его горения раздражающе действуют на оболочки дыхательных путей, а также глаза. Также он может вызвать ожоги, попадая на мокрую кожу.
Реакция на воду спокойная, при неё образуется гидроксид лития и водород. Также характерны реакции с этилом, водородом, и аммиаком. Реакция на серу происходит при 130Вє С, с образованием сульфидов. На углерод реагирует при 200Вє С, в полном вакууме, во время этого образуется ацетиленид. Растворяясь в аммиаке, образует раствор синеватого цвета.
При необходимости длительного хранения литий хранится в отдельных коробках из жести, погружённый в петролинейный эфир или парафин.
Месторождения и добыча лития
Литий представитель литофильных фрагментов ионного происхождения, из них можно отметить цезий, калий и рубидий. К основным минералам, содержащим литий, относятся пироксен, сподумен, слюда и лепидолит. Помимо его нахождения в самостоятельно образованных минералах, его можно обнаружить на месте калия в сторонних соединениях.
Образование лития происходит на почве редкометальных гранитных интрузий, в литиеносных пегматитах или гидротермальных месторождениях, которые помимо лития, в комплексе с вольфрамом, висмутом, оловом и т.д. Наиболее высокая концентрация лития, присуща породам онгонитам – гранитам, содержащих большое количество воды и фтористых образований.
В определённом количестве литий содержит вода в сильносолёных озёрах. Его месторождения имеются в Бразилии, Аргентине, Чили, Канаде, США, Конго, Швеции, Испании, Афганистане, Китае, и Австралии. А также в России, где половина залежей содержащих этот элемент, находится в Мурманской области.
Применение лития
Литий применяется в изготовлении керамики и стеклянной продукции, источников напряжения, горюче-смазочных материалов и полимеров, а также в металлургической промышленности и фармацевтике.
Нередко для устройства требуется мощный и ёмкий аккумулятор. Литий наиболее подходящая составляющая для его изготовления. Если для начинки используется литий, батарея прослужит гораздо дольше. Можно отметить, например, литий-ионный тип подзаряжающихся батарей.
Купить аккумуляторы литийного типа можно двух типов. Разница заключается в используемых электролитах. Литий-ионный аккумулятор – содержит электролит гелевого типа. Модель используется для питания большинства портативной электротехники, в частности, сотовых телефонах, ноутбуках, цифровых фотоаппаратах и видеокамерах.
Литий-полимерный аккумулятор – усовершенствованный вариант первого. В виде начинки используется полимер, содержащий литий. Для устройств имеющих большое потребление энергии, более подходит литий-полимерный вариант.
Также литий добавляют в электролиты других типов аккумулирующих устройств, например, щелочного вида. Это значительно повышает их ёмкость и срок эксплуатации.
Литий, в частности, применяется в металлургической промышленности при изготовления различных необходимых сплавов. Изготовляются сплавы с золотом, серебром, кадмием, магнием, и медью. Эти сплавы нашли своё применение в различных космических и авиационных технологиях.
Для военных нужд, с применением лития, изготовляются керамические элементы для различной техники и особо крепкое стекло. Также он используется в радиотехнических и оптических областях. Литий также применяется в металлогалогеновых лампах.
Идёт этот металл и на медицинские нужды. Доказано, что в небольшом количестве он необходим для нормальной работы организма. Его содержат все внутренние органы. Он участвует во многих обменных процессах и стимулирует иммунитет. Он применяется в препаратах для лечения психологических заболеваний и благотворно сказывается на работе нервной системы.
Цена лития
До 2008 г цена на литий постепенно росли, потом в связи с экономическим кризисом заметно упали. Если в то время цена на килограмм лития составляла порядком 66 долларов, то позже она понизилась с отметки 6,5 тыс. долларов до 5 тыс. долларов за тонну продукта, и после почти не поменялась. Но данные расценки относятся к товару относительно низкого качества.
На более чистый продукт, идущий, например, на изготовление батарей, идёт соответствующая накрутка около 700-800 $. Производители, несмотря на это, предпочитают доплачивать за качество, поэтому доходы от надбавки пока стабильные. Резкого повышения цен в обозримом будущем не ожидается. Чистый литий купить можно будет, приблизительно, за 6 тыс. долларов за тонну.
Прогнозы мирового рынка лития дают определённые надежды на его развитие. Это в основном обусловлено новыми амбициозными проектами в области строения электромобилей, для которых использоваться будут соответственно литиевые аккумуляторы.
С каждым годом этот проект становится всё более реальным, в связи со злободневностью загрязнения окружающей среды выхлопными газами и повышенным спросом на доступные средства передвижения.
Особенно проблема актуальна для развивающихся стран. Но сама технология ещё сырая, в частности, это проблема с хорошими дорогами, и электрическими заправками. Поэтому крупных подвижек на мировом рынке лития в ближайшие годы не предвидится.
ИСЧТОНИК
16
СВОЙСТВА.
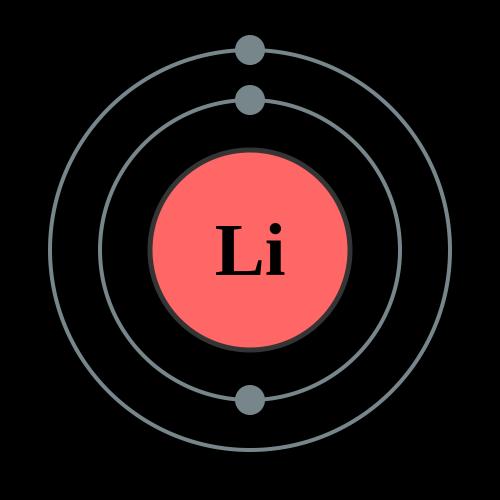
Литий
Литий (Li) — лёгкий редкий металл, атомный номер — 3, атомная масса — 6,94, плотность — 0,534г/см3, температура плавления — 180,5ОС, коэффициент линейного расширения — 168.10-6 (0 — 180ОС), удельная электропроводность — 11,7м/ом.мм2, предел прочности при растяжении — 11,8кг/мм2, относительное удлинение — 50 — 70%.
Литий был открыт в 1817 году шведским химиком Арфведсоном при анализе минерала петалита. Своё название литий получил от греческого “литос”—камень, так как в отличие от щелочных металлов калия и натрия, был обнаружен в каменной породе.
Металлический литий в очень малом количестве был получен в 1818 году, а в 1885 году металлический литий был получен в значительном количестве путём электролиза.
Литий – металл серебристо-белого цвета с жёлтым оттенком, мягок и пластичен как свинец — куётся, прокатывается и протягивается без нагревания.

Литий | 3 | — Raremetal.Ru
Литий — очень лёгкий металл, в два раза легче воды, он плавает в воде и даже в керосине. Очень активно реагирует с водой с бурным выделением водорода, вытесняемым литием из воды. На воздухе окисляется и покрывается белой плёнкой окиси, поэтому хранят его в вакууме или в масле. Обладает высокой теплоёмкостью и теплопроводностью, в жидком виде находится при температурах от 180 до 1327ОС.
Литий расплавляется в воздухе без заметного окисления, а при температуре выше 220ОС — загорается. В сухом воздухе, литий хорошо сохраняется, во влажном — быстро окисляется. Серый налёт при окислении лития — образовавшийся нитрид. Сухой кислород не действует на литий до температуры 200ОС. Сгорая на воздухе, при температуре выше 200ОС, литий образует оксид Li2O. При температуре500-800ОС Li образует с водородом гидрид — LiH.
Литий — редкий металл, в земной коре его в 800 раз меньше чем щелочных металлов калия и натрия. Минералами содержащих литий являются сподумен и лепидолит, в которых содержится от 1 до 3% оксида лития. Кристаллы сподумена достигают массы в несколько тонн. Иногда литий концентрируется в больших количествах в солёных озёрах, в водах нефтяных месторождений, в подземных горячих водах, в районе действующих вулканов. Мировые подтверждённые запасы оксида лития превышают 9 миллионов тонн, а вместе с минерализированными водами — до 30 миллионов тонн.
ПОЛУЧЕНИЕ.
Из минералов сподумена и лепидолита, литий переводится в растворимую хлористую соль (нагревание с мелом и хлористым аммонием), или в сернокислую соль (нагревание с K2SO4), которые, затем, извлекаются с водой.
Полученную соль очищают, переводя её последовательно в LiOH, Li2CO3, а затем в LiCl. Хлористый литий подвергают электролизу в расплаве, со значительным удельным расходом электроэнергии — 50 — 60 тысяч кВтч на тонну лития.
Литий рафинируется переплавкой в масле и отмывкой в бензине. Для более высокой очистки применяется процесс гидрирования лития при температурах 700-800ОС, при которых летит калий, а гидрид лития разлагается при температуре 1000ОС, в вакууме, на чистый литий и водород.
ПРИМЕНЕНИЕ.
В настоящее время литий очень широко применяется в различных отраслях промышленности.
-
Металлургия. Литий является компонентом многих сплавов. В чёрной металлургии литий применяется для раскисления и легирования сплавов. В цветной металлургии литий применяется как раскислитель и дегазатор при плавке меди и её сплавов, как легирующая присадка в сплавах со свинцом и лёгкими металлами. Небольшие добавки (до 0,005%) значительно быстрее и полнее обеспечивают раскисление цветных металлов, хромоникелевой стали и чугуна. Химически активный литий реагирует с кислородом, азотом и серой растворёнными в меди, связывает их и дегазирует медь. Добавки лития к алюминию и магнию повышают их прочность и делают более стойкими к действию кислот и щелочей. В парах лития осуществляется сварка алюминия. Парами лития создают защитную атмосферу в печах для нагревания некоторых металлов, так как литий, реагирует с водяными парами, кислородом и азотом.
-
Применение карбоната лития в виде окатышей в алюминиевой промышленности повышает выход годного металла и уменьшает выделение фтора при производстве алюминия.
-
Хранение и транспортировка водорода. Гидрид лития, выделяющий под действием воды большое количество водорода (3м3/кг), является удобным материалом для хранения и транспортировки связанного водорода.
-
Аккумуляторы. Гидроокись лития применяется в качестве щёлочи в аккумуляторах. Добавка едкого лития в щелочные аккумуляторы значительно повышает их электроёмкость.
-
Вакуумная техника. Металлический литий применяется в вакуумных приборах для получения вакуума. В закрытом сосуде литий поглощает азот и кислород, создавая в нём вакуум. Таким же образом производят очистку аргона и неона от азота, при изготовлении электрических ламп.
-
Термоядерные процессы. Изотоп литий-6 используется для производства трития и применение лития в термоядерных процессах становится всё более значительным. В перспективе, литий как сырьё для производства трития, может стать значительной частью исходного горючего для термоядерных реакторов. Изотоп литий-6 применяется в атомных реакторах, как составная часть материалов защитных экранов против радиации.
-
Очистка воздуха. Хлористый и бромистый литий, а также гидроокись лития хорошо поглощают углекислоту, аммиак, дым и влагу. Кондиционирование воздуха в замкнутых помещениях (подводные лодки, космические корабли) осуществляется с применением соединений лития.
-
Производство стекла и керамики. Соединения лития заменяют свинец при производстве стёкол для кинескопов электронно-лучевых приборов. В производстве стела присадка соединений лития позволяет получать стекло с большой проницаемостью для ультрафиолетовых лучей и малым тепловым расширением. Литий применяется при производстве фарфора, фаянса, термостойкой керамики, огнеупорных и диэлектрических материалов, глазурей и эмалей.
-
Ракетно-космическая техника. Нитратные и перхлоратные соединения лития применяются в качестве окислителей твёрдого ракетного топлива, добавляются к жидкому топливу реактивных двигателей. Жаропрочные соединения лития используются для покрытия сопел и камер сгорания ракетных двигателей.
-
Медицина. Соединения лития( углекислый литий, силициловокислый литий) применяются для растворения мочевой кислоты при лечении подагры.
-
Процессы в звёздах В начальных стадиях жизни звёзд, атомы лития и водорода вступают в термоядерные реакции, образуя бериллий или гелий с выделением большого количества тепла и жёсткого излучения типа рентгеновского.
В настоящее время литий по отраслям промышленности используется в следующем соотношении:
-
керамика и стекло—29%
-
источники тока—27%
-
смазочные материалы—12%
-
непрерывная разливка стали-5%
-
регенерация кислорода—4%
-
полимеры—3%
-
металлургия алюминия—2%
-
другие—16%.
Стоимость лития на мировом рынке
Используемые источники:
- https://xn—-7sbbblh9b0av4l.xn--j1amh/blog/2017/10/08/литий-металл/
- https://pikabu.ru/story/litiy_metall_svoystva_litiya_plyus_video_krasivyikh_reaktsiy_s_litiem_4217215
- https://raremetal.ru/3-li-litij/

 Сульфат Литий - Lithium sulfate
Сульфат Литий - Lithium sulfate Как правильно заряжать литий ионные аккумуляторы
Как правильно заряжать литий ионные аккумуляторы


 Обзор Garmin Fenix 3 Sapphire. Умные часы для активных людей
Обзор Garmin Fenix 3 Sapphire. Умные часы для активных людей 5 практических советов по эксплуатации литий-ионных аккумуляторов
5 практических советов по эксплуатации литий-ионных аккумуляторов Сульфид лития CAS #: 12136-58-2 -ChemWhat
Сульфид лития CAS #: 12136-58-2 -ChemWhat Литий-титанатные аккумуляторы ( LTO ) и его виды
Литий-титанатные аккумуляторы ( LTO ) и его виды